电极界面微观结构对固态锂离子电池性能的影响
摘 要 为了研究固态电解质(SE)孔隙率、裂纹形式以及界面接触面积对于固态电池(SLIB)的影响,利用电阻网络方法对固态电解质(SE)微观结构建模,对SLIB采用一维电化学耦合接触面积模型,建立了一维电化学与二维固态电解质电阻网络模型,并基于该物理模型进行了电化学阻抗谱(EIS)仿真分析。通过不同几何模型来表示电解质缺陷和裂纹,用电阻网络模型计算得到离子电导率,将不同的电解质电导率输入到电池模型中,预测微观结构对于电池容量以及阻抗的影响。研究结果表明,在0°~90°范围内,裂纹角度越小,对SE的电导率影响越小;为了更方便对比裂纹形状对电导率的影响,保持裂纹面积保持不变,随着裂纹长度的生长,电导率损失逐渐上升,到达极值点后,随裂纹长度增加,电导率损失开始下降;裂纹无量纲长度小于0.25时,三角形裂纹造成的电导率损失低于矩形缺陷和椭圆形缺陷;而无量纲长度大于0.25时,三角形缺陷的影响超过矩形缺陷和椭圆形缺陷;随孔隙率增加,SE电导率快速下降,近似呈线性关系。电解质缺陷导致电池的放电电压有所下降,在EIS仿真中体现为体相电阻增加。界面接触面积的损失对于电池容量的损失更为显著,且小倍率放电时,接触面积损失对于容量损失的影响显著低于大倍率放电时。不同接触面积(1.0、0.4)下,比容量下降60.08%,而在大倍率(50 C)时,γ=1.0、0.4时,比容量下降81.95%;倍率较小时,界面面积损失的影响相对较小。界面接触面积损失导致电荷转移阻抗增加,γ从1变化至0.2时,电荷转移阻抗增加25倍,接触面积每损失0.1,电荷转移阻抗平均增加118.60 Ω。与电解质缺陷相比,界面接触面积损失导致的阻抗增加更为明显。在实际应用中,界面接触面积大于0.7,电池才能保证高容量性能。研究仿真了导致SLIB阻抗增加的电解质与界面接触因素,丰富了相关研究。
关键词 固态锂离子电池;界面接触面积比值;电解质裂纹;失效机制;电化学阻抗谱模型
近年来,锂离子电池广泛应用于便携式电子设备与电动汽车中,然而,传统锂离子电池已接近其能量密度极限,无法满足日益增长的储能需求。不可燃的固态电解质(solid electrolyte,SE)替代有机液态电解质是目前提升锂金属电池安全性与能量密度的最佳方式之一。一方面,SE的使用有效解决了电解液泄漏、燃烧、爆炸等问题,还可以有效抑制锂枝晶的生长,另一方面,SE相较液态电解质往往具有较宽电化学窗口,因此,SE可以匹配电压更高的正极材料。
现阶段固态锂离子电池仍然面临着很多问题,其中SE与电极界面的微观结构及界面特性对SLIB性能有显著影响。电池长时间循环导致界面接触面积损失使得锂离子电池性能衰减。Zhang等的研究表明,SLIB多次循环后性能衰减,并观察到电极与电解质界面微观结构发生损伤,在界面处观察到明显的裂纹,该研究将电池性能衰减归因于SLIB界面接触面积的损失。Zhang等研究了锂枝晶生长过程电池性能表现,研究发现,随枝晶生长电解质裂纹逐渐拓展,固态电池性能逐渐下降,这是由于裂纹阻断了SE内离子传输通道。目前的研究大部分集中在裂纹拓展过程以及界面接触面积损失的原因上,而定量描述裂纹以及接触面积对于SLIB影响的研究相对较少。
本工作围绕电解质裂纹和界面特性两方面展开,建立了二维固态电解质电阻网络(resistor network)与一维单离子导体(single ion conductor,SIC)电化学耦合模型,将电解质缺陷以及裂纹以几何模型的方式给出,通过电阻网络模型求解得到电解质离子电导率,将其代入电池模型中通过模拟的方法研究裂纹类型(三角形裂纹、椭圆形裂纹、矩形裂纹)、裂纹角度、界面接触面积对于SE电导率以及电池性能的影响,并通过电化学阻抗谱(electrochemical impedance spectroscopy,EIS)仿真定量描述了界面微观结构对于电池性能衰减的影响。
1 电化学机理模型
本工作建立了一维SLIB数学模型。由于SE离子电导率远低于传统的液态电解质,为了减小锂离子在SE中的传输阻力,通常将电极与电解质设计得很薄,由于正负极以及SE的厚度远小于电池长宽方向的长度,因此,可以将模型沿厚度方向简化为一维。SLIB的正极为非多孔电极LiCoO2,负极为锂金属,SE采用LLZO电解质。充电过程中,锂离子从正极脱出,在锂金属负极表面沉积,与此同时,正极失去电子,正极中的三价钴被氧化,放电过程刚好相反。图1为SLIB结构,坐标x=0处为锂金属电极和SE界面,x=L1处为SE与正极界面。

图1 SLIB结构
正负极反应方程式如下:
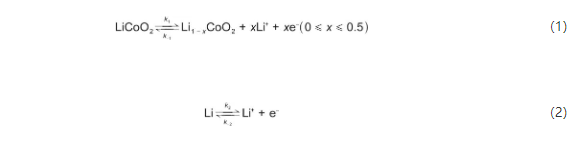
1.1 电化学反应动力学方程
1.1.1 正极反应电化学反应动力学方程
正极-SE界面反应可由Butler-Volmer方程表述:
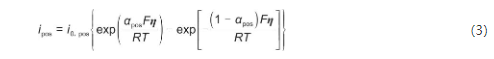
式中,ipos为正极局部电流密度,A/m2;αpos为正极传递系数;R为气体常数,R=8.314 J/(mol·K);T为温度,K;F为法拉第常量,C/mol。
本工作采用的Fabre模型中,认为SE中的锂离子浓度是均匀的,同时考虑到正极与电解质界面不完全接触的影响,在一维电化学模型中引入实际接触面积与名义接触面积之比(γ=A/A0),对参考交换电流密度i0, pos修正如下:
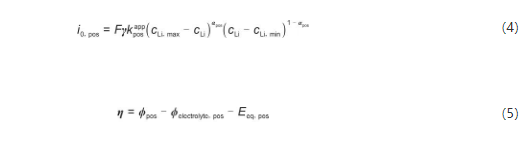
式中,Eeq, pos采用COMSOL材料库中的插值函数,V;ϕelectrolyte, pos=ϕ(L1,t),为x=L1处的电解质电势,V;ϕpos为正极电势,V;i0, pos为正极交换电流密度,A/m2;γ为实际接触面积与名义接触面积之比;η为过电势,V;cLi, max与cLi, min分别是正极中Li最大和最小浓度,mol/m3;k图片为正极反应的表观速率常数,mol/(m2·s)。
1.1.2 负极反应电化学反应动力学方程
锂金属质地较软,且已有文献表明,在施加压力时有蠕变效应产生,因此,可以认为负极完全接触,不考虑接触面积损失的影响。负极界面反应的Butler-Volmer动力学方程如下:
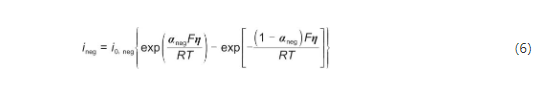
式中,ineg为负极局部电流密度,A/m2;αneg为负极传递系数。SIC模型中,i0, neg修正为:

式中,ϕelectrolyte, neg=ϕ(0,t),负极接地,因此ϕneg=0 V;k图片为负极反应的表观速率常数,mol/(m2·s);ϕelectrolyte, neg=0,为负极和电解质界面电势,V;Eeq, neg=0,为负极平衡电势,V。
1.2 双电层修正正负极反应
在固态电解质与电极接触界面上,存在双电层(electrical double layer),通过电极与电解质界面的电流可以分为两部分:①驱动电荷转移反应的电荷转移电流(ict);②用于双电层的充放电的双电层电流(idl)。
在电极与固态电解质界面,外部施加电流密度与两者的关系满足:

式中,ibat为电池的电流密度,A/m2;ict为电荷转移电流,A/m2;idl为双电层电流,A/m2。
其中,idl表达式如下:

将以上关系式代入,得到

式中,cdl, pos为正极双电层电容,F/cm2;cdl, neg为负极双电层电容,F/cm2。
1.3 物质守恒
1.3.1 正极控制方程及边界条件
由于正极中存在浓度梯度,因此会产生LiCoO2扩散以及迁移。正极内部控制方程可由式(13)得到:

式中,cLi为Li在正极中的浓度,mol/m3;jLi为LiCoO2在正极中的质量通量,mol/(m2·s);t为时间,s;RLi为正极与电解质界面处的反应速率,mol/(m3·s)。电极中LiCoO2通量可由式(14)计算得到:

式中,DLi为正极LiCoO2扩散系数,m2/s。
因为是恒流放电过程,总电流不受接触面积减小的影响,界面Li的反应速率会相应增大,因此对界面反应速率进行修正,考虑到接触面积比γ,修正为:

式中,γ为实际接触面积与名义接触面积之比;Zi为电极反应化学计量系数;n为参与反应电子数。
正极两侧边界条件如下:

1.3.2 固态电解质中的控制方程及边界条件
SIC模型假设电解质中只有一种离子移动,由于电中性假设,因此电解质内没有浓度梯度,因此控制方程:

式中,c为SE内锂离子浓度,mol/m3。
1.4 电荷守恒
在放电过程中,固态电池系统的电荷处于守恒状态,由于Li+在固相中传输,其电流密度可用欧姆定律来描述:
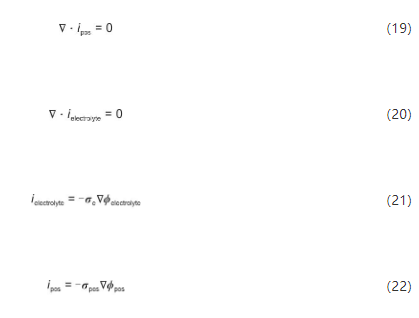
式中,ielectrolyte、ipos分别为SE、正极中的电流密度,A/m2;σe、σpos分别为SE离子电导率、正极的有效电导率,S/m;ϕelectrolyte、ϕpos分别为固态电解质和正极的电势,V。
1.5 微观结构及裂纹建模
为研究电解质微观结构对电导率的影响,建立了电解质微观模型。为了简化计算,SE内晶粒结构简化为二维正方形,如图2所示,黑色线条为晶界,晶粒内部以及晶界的导电性具有各向同性,黑色正方形或三角形区域为空位,该区域的导电性远低于晶粒和晶界。
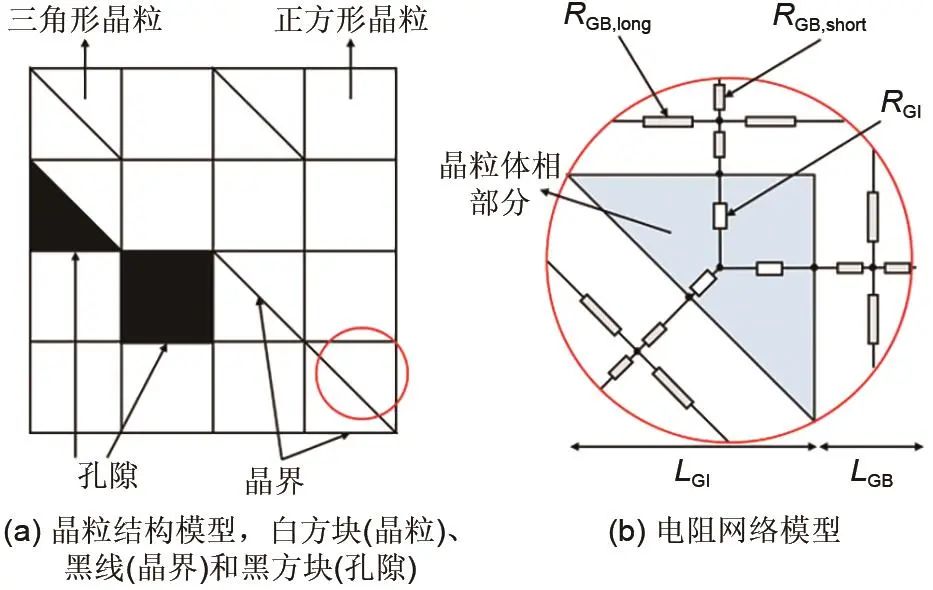
图2 SE晶粒结构模型和电阻网络模型
图2(b)中的RGB, long、RGB, short和RGI分别为沿晶界长度方向的电阻、沿晶界宽度方向的电阻、晶粒电阻,Ω。计算公式如下:

式中,LR为图中电阻的长度,m;σ为电导率,S/m;AR为截面积,m2。
使用节点电流法,对每个节点的电流求和,节点电压由式(24)、(25)计算得到。
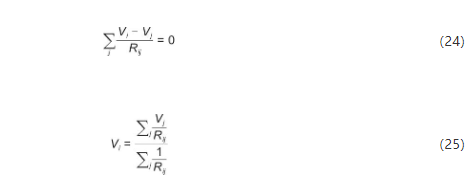
式中,Vi代表节点i的电压;j为和i节点直接相连的节点;Rij为节点i和j之间的电阻,Ω。由电阻网络法求得离子电导率后,由Nernst-Einstein方程求得锂离子扩散系数:

式中,D为电解质内离子扩散系数,m2/s;kB为玻尔兹曼常数,kB=1.380649×10-23 J/K;e为基本电荷量,C;n为移动离子密度,m-3。
实验和仿真的结果表明,裂纹产生和拓展具有很大的随机性,目前裂纹生长的模拟方法主要采用相场方法,但是本工作旨在研究裂纹对于电解质的影响,因此,裂纹形状以边界条件的形式给出,如图1所示,根据文献[7]中的研究,将裂纹等价成椭圆形、三角形、长方形3种不同形状。
图3为存在裂纹的SE电阻网络模型,左侧边界为负极与SE的界面,右侧为正极与SE的界面,其中(a)~(c)的局部放大图分别表示三角形裂纹、椭圆形缺陷和矩形缺陷的几何结构。裂纹角度的定义如图3(a)所示,左界面设为y轴,三角形在y轴上的底边中点为原点,底边中线与y轴的角度β即为裂纹角度,中线方程y=xcotβ;裂纹高度的定义如图3(b)所示,椭圆方程为x2/b2+y2/a2=1,椭圆的长半轴长为裂纹顶点与左界面之间的距离L=b,即裂纹高度,椭圆形裂纹的面积为abπ/2。
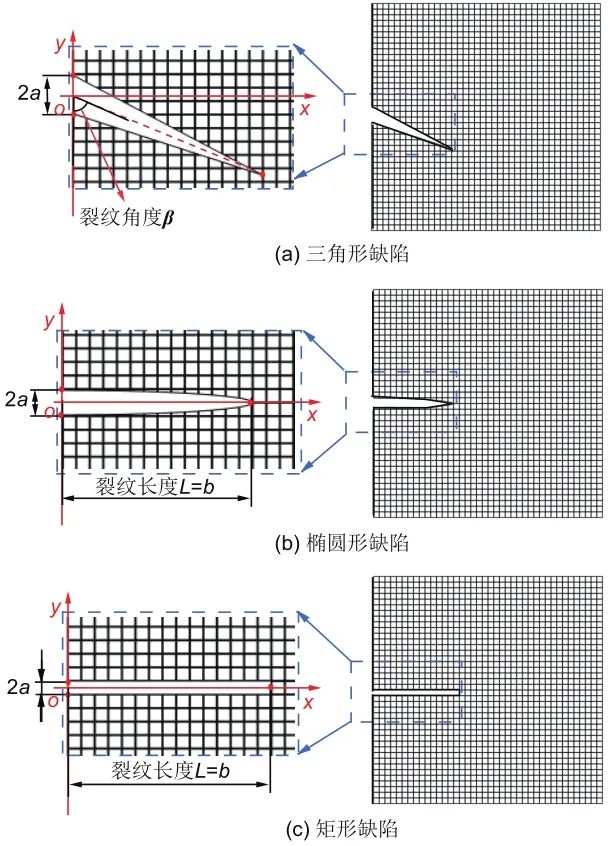
图3 存在裂纹的SE电阻网络模型图
如图3所示,裂纹区域不存在晶粒,电阻网络模型只在晶粒上求解,即裂纹区域不求解电阻网络模型,由于制备以及循环过程中,SE中的裂纹可能会被锂金属填充,为了模拟裂纹的界面,裂纹与电解质的界面电压设置为0 V。裂纹面积会对SE的电导率产生影响,为了研究不同形状裂纹对于离子电导率的影响,本节在计算中保持不同形状裂纹的面积相同,来研究不同形状、高度对于离子电导率的影响。
电解质两侧施加的电压分别为正负极与电解质界面的电压,由于锂负极接地,锂金属电导率较高,且薄膜电池中锂金属负极厚度在微米级,一般认为电解质与锂金属界面电压与接地电压相等,因此,负极与电解质界面的电压取0,正极/电解质界面电压由电化学方程组计算得到,通过计算得到的电流,计算出电解质的电导率。由于本工作采用的SIC模型,采用欧姆定律描述电解质电流,因此无需通过Nernst-Einstein方程计算扩散系数,与Danilov的模型相比,更易耦合电解质微观结构模型。
1.6 EIS模拟
电池阻抗响应模拟频率0.1~106 Hz,交流信号振幅5 mV,阻抗测量期间,电池电压保持在4.0 V,因此,EIS仿真中,将电池初始值设置为4.0 V,将相同的扰动电压信号应用于电化学机理模型中,分析模型的输入以及输出信号获得相应的EIS响应。
EIS模拟中,对于施加一个扰动电压,表达式 如式(27):

式中,图片为正常工作电压,V;图片为谐波扰动电压的振幅,V;ω为频率,Hz;j为-1的平方根。电池电流密度的相应响应表达式如下:

式中,图片为正常工作电流密度,A/m2;图片为由于谐波电压扰动引起的电流扰动幅度,A/m2;ψ为谐波电流相对于谐波电压扰动的相位差,V。上式两侧同乘expj(ωt),在一个周期τ内进行积分,得到 式(29):
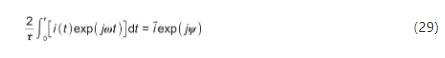
从上式中可以获得电流谐波扰动和相位差。
STFLIB涉及的物理过程基本上是非线性过程。当周期性电压扰动叠加到电池工作电压上时,电池状态将围绕该点振荡。扰动大小足够小时,电池物理过程可以被视为线性。在这种情况下,可以使用电压与电流的比值计算阻抗:
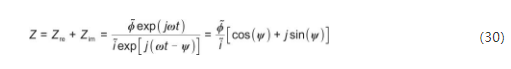
式中,Z为锂离子电池的阻抗,Ω;Zre为阻抗实部,Ω;Zim为阻抗虚部,Ω。
通过上式可以计算电池的电化学阻抗谱特性,由此反映出电池的电化学反应过程、材料特性等参数。
1.7 模型求解
本工作的求解思路如图4所示。
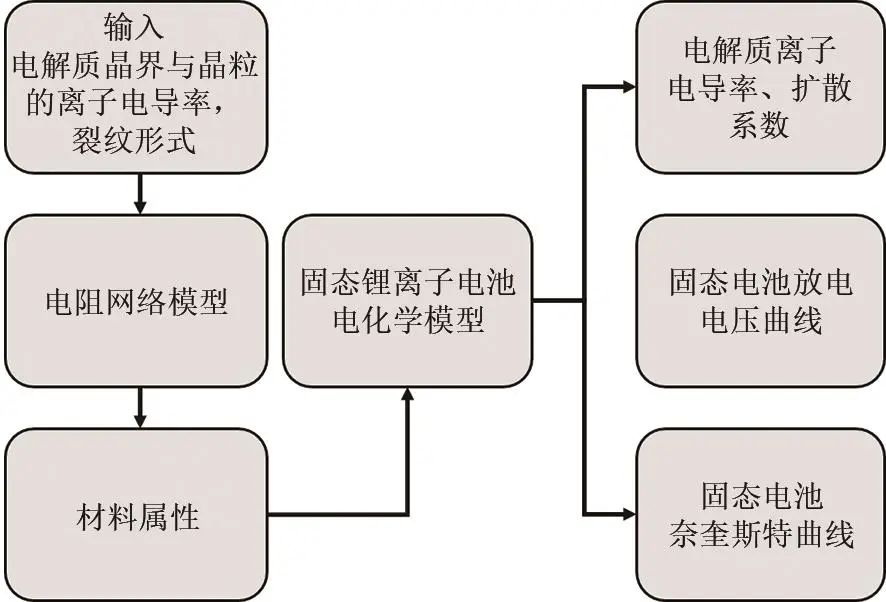
图4 本工作计算流程
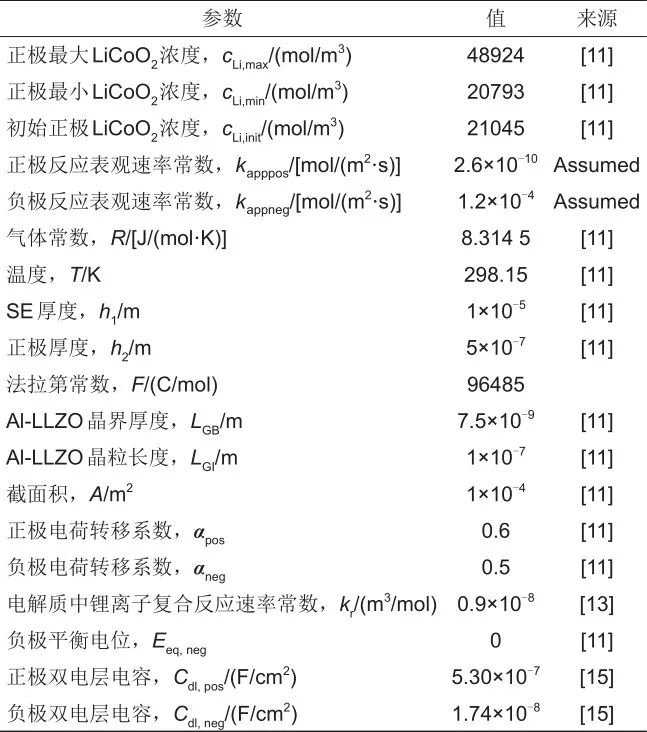
采用有限元方法对上述模型进行离散化,模型求解使用商业软件COMSOL Multiphysics 6.0,收敛残差为10-4,在64位Windows平台、32 GB RAM和AMD 3800X 3.90 GHz 8核处理器上计算时间约为60 s。模型中相关参数取值列于表1,部分电池结构参数取自文献[11]与文献[15]。
表1 模型参数
1.8 模型验证
图5(a)是10 C放电倍率时,本工作SIC模型放电曲线和参考文献[11]中放电曲线对比,从图中可以看出,放电阶段前期电化学模型吻合较好,在放电阶段末期误差小于7%,图5(b)是不同倍率下放电容量对比,从图中可以看出,小倍率放电时,SIC模型比容量更高。
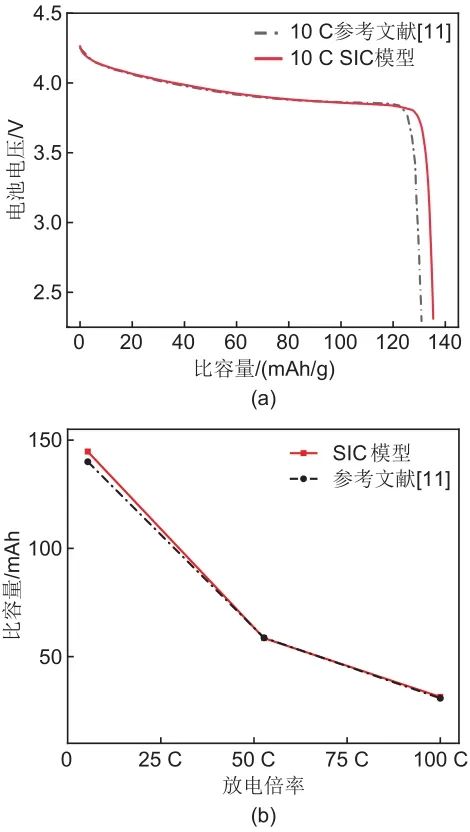
图5 (a) 本工作模型10 C放电曲线和参考文献中放电曲线对比图;(b) 不同放电倍率下放电容量对比图
2 结果和讨论
2.1 孔隙率与界面接触面积对固态电池性能的影响
图6(a)为不同倍率下,界面实际接触面积与比容量的变化曲线,由图可知,小倍率放电时,比容量与实际接触面积呈现线性关系,而在大倍率放电时,呈现非线性变化,这可能是由于在大倍率放电时,固固界面的离子通道数量限制了电池放电过程;放电倍率较低时流经界面的电流也较小,因此接触面积对于电池性能的影响相对较小。图6(b)为电解质孔隙率变化时,电池放电电压曲线变化,由图可知,孔隙率增大时,由于电导率的下降,整个电池的内阻增加,因此,电池电压下降,电池比输出功率也会下降,但是电池的比容量并没有减小。
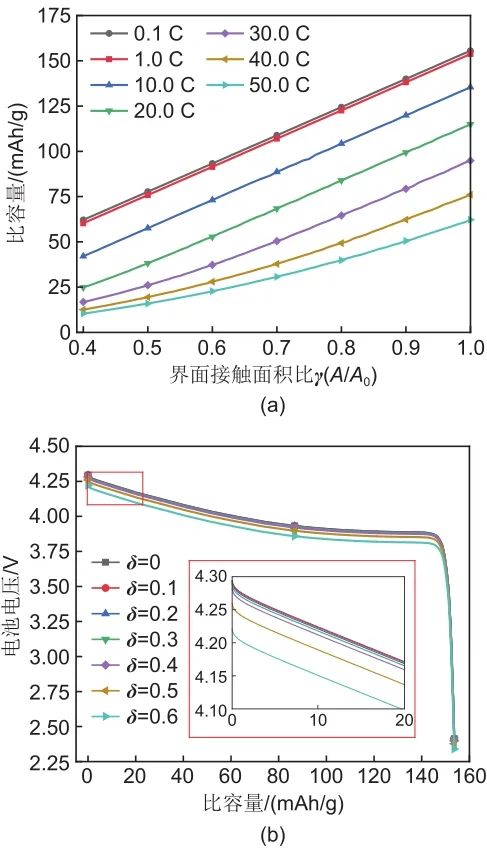
图6 (a) 不同倍率下界面接触面积与容量损失的关系;(b) 电解质孔隙率与放电曲线关系
图6比较了不同倍率、不同接触面积以及不同孔隙率对电池放电曲线的影响,研究表明,高倍率放电以及界面损失均会造成电池比容量的损失;小倍率(0.1 C)放电时,不同接触面积(1.0、0.4)下,比容量从155.56 mAh/g下降至62.10 mAh/g,下降约为60.08%,而在大倍率(50 C)时,γ=1.0、0.4时,比容量从31.43 mAh/g下降至5.67 mAh/g,下降约为81.95%。倍率较小时,界面面积损失的影响较小。

